四川腸道菌群移植適用人群
腸道菌群移植對多藥耐藥菌和耐藥基因有何長期影響?
1通過培養(yǎng)組學和宏基因組學,探究糞菌移植對多次復發(fā)的艱難梭菌患病患者中多重耐藥(MDR)細菌和抗性基因的影響;
2短期內(nèi)(3周后),MDR細菌的定植率下降11.5%,而基于糞便宏基因組測序,發(fā)現(xiàn)ARG相對豐度有所減少;
3與健康捐贈者相比,患者體內(nèi)不同ARG的數(shù)量仍然較高,且抗性質(zhì)粒的水平似乎不受FMT影響;
4長期來看(1-3年),受體的抗性基因組仍類似于捐贈者,表明FMT的效果可能持續(xù)數(shù)年。 菌群移植過程中,保持菌群的活性與多樣性是關鍵!四川腸道菌群移植適用人群
菌群移植(Fecalmicrobiotatransplantation,F(xiàn)MT)當時被用于改善rCDI,有效率超過90%,目前已被臨床醫(yī)學指南及共識推薦用于復發(fā)性或難治性CDI,并逐漸推廣應用于慢性constipati、腹瀉、腸易激綜合征(Irritablebowelsyndrome,IBS)和炎性腸病(Inflammatoryboweldisease,IBD)等腸道功能性和器質(zhì)病變以及神經(jīng)精神系統(tǒng)(自閉癥、焦慮、抑郁癥和帕金森病)、代謝系統(tǒng)和tumour免疫診療等。以上疾病病因復雜且傳統(tǒng)的藥物診療效果非常有限,應用FMT技術診療卻獲得了大部分的療效認可。FMT診療constipati患者的變好率較常規(guī)診療可提高3倍以上;IBD可以獲得較長時間的臨床完全緩解,特別是針對年輕的IBD患者以及克羅恩病患者,F(xiàn)MT的緩解率超過60%;糞便菌群移植2年后,自閉癥癥狀減輕了近50%。FMT診療是一種創(chuàng)新的、具有明確臨床意義的診療方案,甚至被認為是新療法!陜西研究菌群移植安全性菌群移植哪家專業(yè)?上海沃本,用科技守護您的腸道微生態(tài)!

在根特大學的雙盲試驗中,接受健康供體FMT的患者運動功能改善。“他們動作更敏捷,僵硬感減輕,穿衣吃飯不再費力。”根特大學神經(jīng)學家Patrick Santens描述道。令人意外的是,連安慰劑組(移植自身菌群)也有2.7分的提升,暗示腸道環(huán)境本身對癥狀存在復雜調(diào)控。目前,Santens團隊正分析供體菌群特征,試圖鎖定“關鍵菌種”,并計劃于2026年啟動更大規(guī)模試驗。
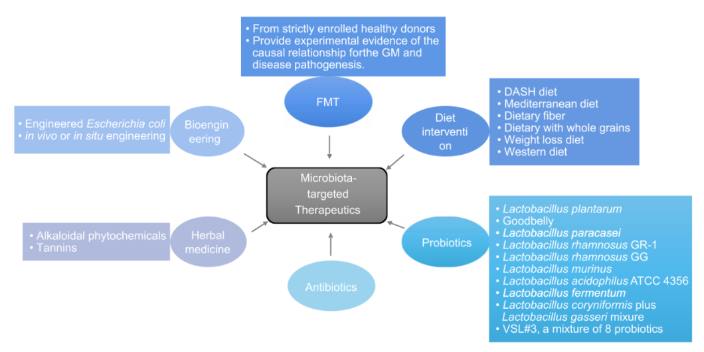
未來療法:精細干預還是阻斷機制?科學家們正從兩條路徑推進研究:一是通過膳食纖維補充、FMT等手段重塑菌群平衡;二是針對微生物群觸發(fā)的病理機制開發(fā)靶向藥物。例如,加州大學團隊發(fā)現(xiàn),大腸桿菌在炎癥環(huán)境中會氧化多巴胺,促使α-突觸**白聚集,而咖啡酸可阻斷這一過程;另一團隊則從綠茶提取物中找到了抑制致病蛋白“Curli”的方法,相關藥物已進入研發(fā)階段。盡管前景光明,謎團依然存在。帕金森病可能存在“腸道優(yōu)先”和“大腦優(yōu)先”兩種亞型,而菌群干預對哪類患者更有效?長期追蹤數(shù)據(jù)仍匱乏。美國NIH資助的“腸腦軸”研究聯(lián)盟正試圖填補這一空白,計劃對患者菌群變化進行多年跟蹤。
鄭州大學第二附屬醫(yī)院團隊揭示了干擾素基因刺激因子(STING)在糞菌移植(FMT)應用小鼠潰瘍性結(jié)腸炎中的關鍵作用,發(fā)現(xiàn)STING依賴方式可改善炎癥性腸病患者的免疫失衡狀態(tài)。2通過比較不同STING表達水平的小鼠在接受FMT應用后的效果差異,發(fā)現(xiàn)FMT療法以STING依賴的方式緩解DSS誘發(fā)的結(jié)腸炎;3機制上,F(xiàn)MT通過STING調(diào)控腸道Th17細胞和巨噬細胞、脾臟Th1和Th2細胞以及腸系膜淋巴結(jié)Th1細胞的分化,下調(diào)結(jié)腸M1/M2和脾臟Th1/Th2細胞比例,從而緩解癥腸炎的免疫失衡狀態(tài);4同時,STING可促進供體菌株尤其是乳酸菌屬在受體腸道中的定植,從而重塑結(jié)腸炎中失調(diào)的腸道菌群;5本研究表明STING作為FMT應用的關鍵靶點,或可成為篩選適合接受FMT應用個體的生物標志物,以優(yōu)化應用方案并提高臨床益處。重塑腸道健康,菌群移植選上海沃本。
早在2003年,神經(jīng)解剖學家Heiko Braak提出假說:帕金森病可能始于腸道。某種病原體通過迷走神經(jīng)侵入大腦,而α-突觸蛋白的異常聚集正是這一過程的“路標”。后續(xù)研究佐證了這一猜想——排便困難患者數(shù)十年后患病風險更高,而切除闌尾或切斷迷走神經(jīng)的人群風險降低。更關鍵的是,動物實驗顯示,無菌環(huán)境中的轉(zhuǎn)基因小鼠(易產(chǎn)生α-突觸蛋白)運動癥狀出現(xiàn)更晚;移植帕金森患者的腸道菌群后,小鼠癥狀甚至加劇。
“即便病理不始于腸道,癥狀終將蔓延至此。緩解腸道問題本身就有價值,若能延緩疾病進展,更是錦上添花。” 菌群移植技術正逐步走出實驗室,進入臨床應用階段。山東小腸菌群移植成功案例
研究顯示,菌群移植在改善腸道健康方面展現(xiàn)出巨大潛力!四川腸道菌群移植適用人群
近年來,隨著人口老齡化進程不斷加快,人民慢性病疾病負擔日益沉重,成為影響國家經(jīng)濟社會發(fā)展的重大公共衛(wèi)生問題。例如,我國的constipation患者超過2億;我國IBD患者近十年的發(fā)病人數(shù)達到前面十年的2.5倍,目前預計約有150萬患者;我國消化道疾病特別是Colorectalcancer呈現(xiàn)快速增加的趨勢,每年Colorectalcancer的發(fā)病人數(shù)達到37.6萬人,且仍在以4.2%的速度快速增長;我國自閉癥現(xiàn)存人群約有1000萬;我國抑郁癥人群近6000萬;我國超重和肥胖患者達到3億人,其中肥胖患者超過9000萬。目前的研究發(fā)現(xiàn)腸道菌群與慢性疾病之間存在緊密聯(lián)系,菌群移植可以通過人為調(diào)節(jié)人體腸道微生物達到緩解疾病的目的,極具臨床應用前景!四川腸道菌群移植適用人群
- 甘肅腸道菌群移植機構(gòu) 2025-06-14
- 陜西腸道菌群移植的效果 2025-06-14
- 山東小腸菌群移植適用人群 2025-06-14
- 山西自體菌群移植**共識 2025-06-14
- 江西腸道菌群移植耗材 2025-06-14
- 山東腸道菌群移植成功率高嗎 2025-06-14
- 江西自閉癥使用菌群移植臨床應用 2025-06-14
- 江蘇腹瀉使用菌群移植費用 2025-06-14
- 浙江自體菌群移植適用人群 2025-06-14
- 河南常見菌群移植耗材 2025-06-14
- 溫州本地試劑盒怎么用 2025-06-14
- 深圳養(yǎng)老院共享輪椅廠家 2025-06-14
- 國產(chǎn)牙托粉費用 2025-06-14
- 外泌體公司公司 2025-06-14
- 除顫儀醫(yī)療設備培訓教育保障 2025-06-14
- 山西腰部固定器要多少錢 2025-06-14
- 廣東國產(chǎn)全自動核酸提取儀廠家批發(fā)價 2025-06-14
- 河南新世紀牙托粉費用 2025-06-14
- 子午流注產(chǎn)品治未病服務適宜技術產(chǎn)品目錄 2025-06-14
- 洗鼻器銷售公司 2025-06-14