長寧區pH電極執行標準
pH 電極健康管理領域的應用,人體體液的 pH 值對維持正常生理功能至關重要。例如,血液 pH 值通常維持在 7.35 - 7.45 之間,偏離這個范圍可能引發各種疾病,如呼吸性堿中毒、腦損傷和腎結石等。通過使用 pH 電極實時監測人體體液(如血液、汗液、尿液等)的 pH 值,有助于及時發現潛在的健康問題。如利用可穿戴設備集成氧化銥納米線固態 pH 電極,可實現運動過程中人皮膚表面 pH 值的動態監測,為運動健康管理提供數據支持,能夠提早發現身體中的異常及情況,提前做出預警預防。pH 電極工業控制系統需設置電極失效預警,避免生產事故風險。長寧區pH電極執行標準

特定氧化物對玻璃膜性質及pH電極性能影響的量化研究——Li?O 的影響。1、對玻璃膜結構與性質的影響:Li?O 的加入能夠打破玻璃網絡結構中部分 Si - O 鍵,使玻璃網絡結構變得相對疏松。這是因為 Li?離子半徑較小,電荷密度相對較高,能夠吸引玻璃網絡中橋氧離子的電子云,削弱 Si - O 鍵的強度。從量化角度來看,隨著 Li?O 含量的增加,玻璃的結構參數如平均非橋氧數(NBO/T)會發生變化。例如,在一定基礎玻璃配方中,當 Li?O 含量從 x?% 增加到 x?% 時,NBO/T 值可能從 y?增加到 y? 。2、對電極性能的影響:這種結構變化會影響離子在玻璃膜中的傳輸。Li?離子在玻璃膜中具有較高的遷移率,能夠為 H?離子的傳輸提供更多的通道。研究表明,適量 Li?O 的添加可提高電極的響應速度。在對某一 pH 范圍溶液進行測量時,未添加 Li?O 的電極響應時間可能為 t?秒,而添加適量 Li?O 后,響應時間可縮短至 t?秒(t? < t?)。同時,Li?O 的添加還可能影響電極的選擇性。當溶液中存在其他干擾離子時,添加 Li?O 的電極對 H?離子的選擇性系數可能會發生變化,例如從 K?增加到 K? ,表明其對 H?離子的選擇性增強。安徽pH電極詢問報價便攜式pH 電極內置溫補功能,適應野外測量場景。
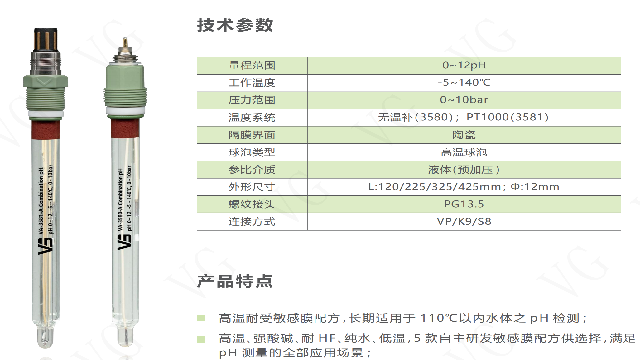
影響pH 電極玻璃膜電位形成的因素。玻璃膜的組成成分對其性能有較大影響。不同的玻璃配方會導致膜的離子選擇性、響應速度和穩定性不同。例如,增加玻璃中二氧化硅的含量可以提高膜的化學穩定性,但可能會降低對 H?的響應靈敏度;而引入一些堿金屬氧化物可以改變膜的離子交換特性,影響對 H?的選擇性。此外,溶液中的離子強度、溫度以及共存離子等因素也會干擾膜電位的形成,進而影響測量準確性。溶液離子強度的改變會影響 H?的活度系數,導致測量的 pH 值出現偏差;溫度的變化不僅影響能斯特方程中的系數,還可能改變玻璃膜的物理化學性質,如膜的電阻等。
基于 IGZO 的 pH 電極:In - Ga - Zn - O(IGZO)近年來被廣泛應用于 TFT 基板以替代 α - Si。在相關研究中,將 70 nm 厚的 IGZO 層直接沉積在 P 型 Si 襯底上作為傳統擴展柵場效應晶體管(EGFET)的擴展柵,用作 pH 傳感膜。通過在不同溫度下進行沉積后退火(RTA)處理,可改善 IGZO 層的 pH 傳感性能。例如,在 N?氣氛中 700℃下進行 RTA 處理,在 pH 2 - 10 的應用范圍內,靈敏度可從 41.5 mV/pH 提高到 53.3 mV/pH 。此外,改變 RF 濺射過程中的 Ar/O? 比例也會影響電極性能,如在 Ar/O? 氣氛為 24/1 的條件下制備的 IGZO - EGFET 具有靈敏度(59.5 mV/pH)和線性度(99.7%),且在 7 個月后仍能保持較高性能(靈敏度 51.4 mV/pH,線性度 92%)。環保監測中,pH 電極實時傳輸水質數據至平臺。

pH 電極:工業物聯網的智能感知節點,在工業物聯網的蓬勃發展中,pH 電極作為智能感知節點,為工業生產的智能化升級注入了新的活力。基于其對溶液 pH 值的快速、準確測量原理,pH 電極與物聯網技術深度融合。在化工、制藥等行業的生產線上,pH 電極實時采集反應體系或工藝流程中的 pH 值數據,并通過物聯網網絡將數據傳輸至云端或本地服務器。企業管理人員和技術人員可以通過手機、電腦等終端設備實時查看 pH 值數據,實現遠程監控和管理。同時,結合大數據分析和人工智能技術,根據 pH 值數據預測生產過程中的潛在問題,提前采取措施,優化生產流程,提高生產效率和產品質量。pH 電極憑借其智能化的感知能力,成為工業物聯網中不可或缺的重要組成部分。pH 電極運輸時需用原裝包裝盒,避免電極頭碰撞導致膜層破損。馬鞍山品牌pH電極
pH 電極測膠體樣品時,建議選用大孔徑液接界防止堵塞。長寧區pH電極執行標準
pH 電極玻璃膜的構成原理,pH 電極玻璃膜通常由特殊組成的玻璃制成,其對氫離子具有選擇性響應。當玻璃膜與溶液接觸時,在膜表面發生離子交換過程。玻璃膜內含有可與溶液中氫離子進行交換的離子位點,如鈉離子等。當膜浸入溶液中,溶液中的氫離子與玻璃膜表面的離子進行交換,在膜表面形成一層水化凝膠層。在這一過程中,膜內外的離子活度不同,從而產生膜電位。膜電位的形成可以用能斯特方程來描述,其表達式為:E=E0+nF2.303RTlogaH+,其中E為膜電位,E0為標準電極電位,R為氣體常數,T為固定溫度,n為離子電荷數,F為法拉第常數,aH+為氫離子活度。這表明膜電位與溶液中氫離子活度的對數呈線性關系,通過測量膜電位就可以確定溶液的 pH 值。長寧區pH電極執行標準
- 那種pH電極廠家報價 2025-06-10
- 四川中型pH自動控制加液系統 2025-06-10
- 耐腐蝕pH傳感器 2025-06-10
- 數字pH電極內容 2025-06-10
- 河北科研院所用pH自動控制加液系統 2025-06-10
- 泰州pH電極執行標準 2025-06-10
- 金山區pH電極耗材 2025-06-10
- 鹽城電子pH電極 2025-06-10
- 氯堿化工用pH傳感器品牌 2025-06-10
- 蚌埠有哪些pH電極 2025-06-10
- 紹興溫度試驗試驗機 2025-06-10
- 怎樣選擇液相色譜哪個好 2025-06-10
- 在線式測溫紅外測溫儀批發價格 2025-06-10
- 佛山相機鏡片哪家好 2025-06-10
- 浙江磁芯表面絕緣層涂覆過濾用濾芯價目表 2025-06-10
- 泰州電力設備數據采集與監控系統商家 2025-06-10
- 西藏斑馬魚模式動物儀器廠家 2025-06-10
- 天津工業級纖維直徑報告系統 2025-06-10
- 快插接頭重慶接頭型號 2025-06-10
- 上海細菌菌落計數分析儀 2025-06-10